|

- 现金
- 222032 元
- 精华
- 285
- 帖子
- 67620
- 注册时间
- 2001-11-10
- 最后登录
- 2023-5-7






















|
本帖最后由 风雨不动 于 2012-4-14 07:40 编辑
抗逆转录病毒药物耐药性的发生
来源: 医学论坛报
发布: 2011-8-27
无论哪种病毒亚型,抗逆转录病毒药物的联合(使用)在治疗人类免疫缺陷病毒(HIV)感染方面均有效。然而,各种HIV变异体对抗逆转录病毒药物的耐药水平不同。事实上,我们对1型HIV(HIV-1)非B亚型的耐药突变及其临床关联性的了解有限,尽管事实上全世界90%以上的HIV-1感染病人有HIV-1的非B亚型变异体。大多数有关药物耐药性的报告都涉及发达国家中的 B亚型感染。酶学数据和病毒学数据均表明,不同HIV亚型中自然发生的多态性可以影响HIV-1对各种抗逆转录病毒药物的敏感性以及HIV获得特定耐药突变的倾向。此外,不同亚型的耐药途径有可能影响药物的交叉耐药性以及特殊二线治疗方案的可能使用。在发展中国家这种担心有可能增加。大量的自然遗传变异已导致M群(主要)HIV-1细分为9个亚型(A~D,F~H以及J和K)和大量的流行重组型(CRFs),例如CRF01_AE和 CRF02_AG1-3。虽然在西方国家B亚型最流行,但在其他地区以非B亚型为主(例如撒哈拉以南非洲、印度和巴西部分地区的C亚型;东南亚的 CRF01_AE亚型;西非的CRF02_AG亚型;以及东欧和亚洲北部的A亚型1,4,5)。由于移民,非B亚型的比例在北美和南美以及西欧正日益增高 6-9。
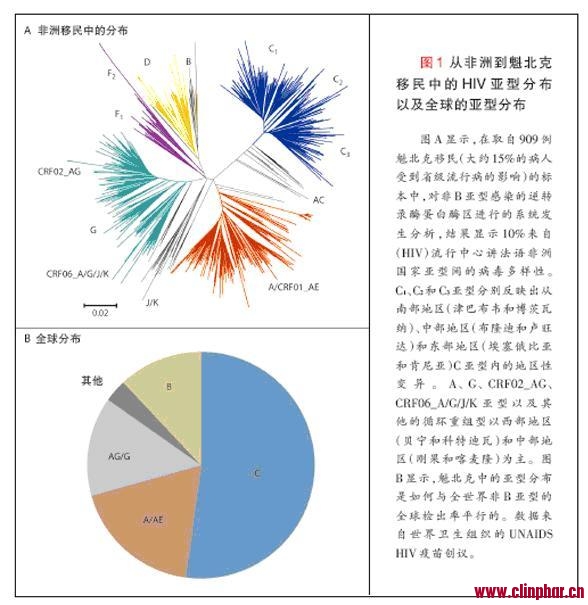
尽管抗逆转录病毒治疗的进展已使HIV管理发生了革命性变化,并且地区性疾病流行的蔓延已得到控制10-12,但在使用这类药物的所有地区都已出现了对抗逆转录病毒药物的耐药性。除了B亚型以外的亚型中,该话题尚未得到充分研究,因为在最早引入抗逆转录病毒药物的富裕国家中以后者(B亚型)为主,而且在这类地区可以获得抗逆转录病毒药物耐药性的基因型和表型检测13。然而,可产生赋与耐药突变不同模式的亚型间基因差异的可能性,受到HIV亚型在基因内容方面发生自然变异的支持—— 例如病毒包膜(env)基因中40%的变异,以及聚合酶(pol)和组特异性抗原基因(gag)中8%~10%的变异。该问题由于以下事实而具有特殊意义:HIV pol基因可编码逆转录酶、蛋白酶和整合酶酶类(是抗逆转录病毒治疗的主要靶点)中的每一种。从处于HIV大流行中心的非洲国家到(加拿大)魁北克的移民中,HIV亚型的分布可以说明逆转录酶—蛋白酶区的亚型间和亚型内多样性14 (图1A)。(HIV)大流行的全球蔓延和多样化显示C亚型(48%)、A亚型和CRF01_AE亚型(分别为12%和5%)以及G亚型和CRF02_AG亚型(分别为8%和5%)的主要疾病流行(图1B)2,3。
28 分钟前 上传
下载附件 (145.69 KB)
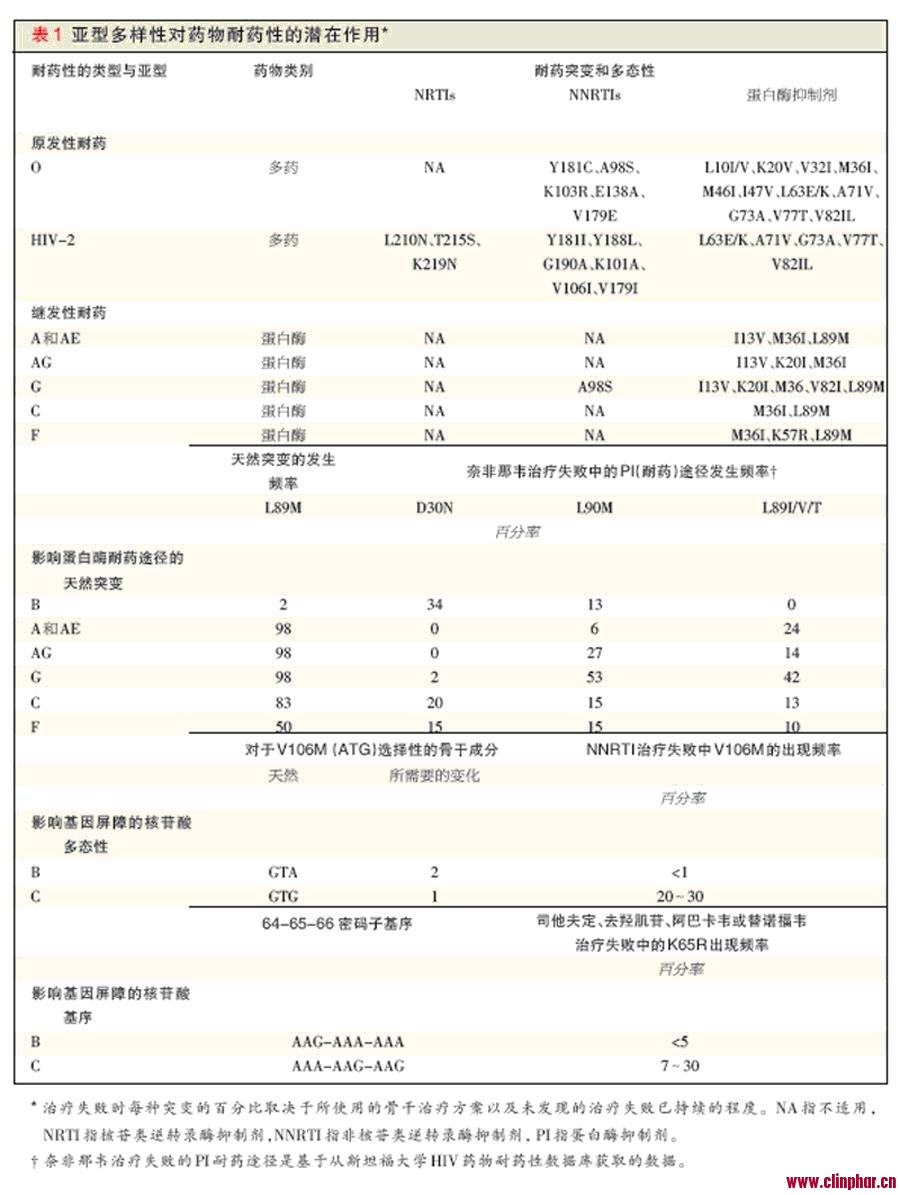
与耐药突变相关部位上的密码子序列差异,或许使不同亚型的病毒分离株偏向于编码不同的氨基酸取代,后者可能影响耐药性的出现率(表1,见下期)13,15。这种多样性还可能影响同类抗逆转录病毒药物间的交叉耐药性,从而可能影响抗病毒的疗效反应和临床转归(参见相互作用图,其与本文全文均可从NEJM.org获取)13。
生化数据和病毒学数据表明,氨基酸的自然变异可影响某些耐药突变所赋与耐药性的强度16。例如,因为以一种天然多态性出现的逆转录酶突变,所以相关的2型HIV(HIV-2)病毒和O群 HIV-1病毒显示出对某些非核苷类逆转录酶抑制剂(NNRTIs)的高水平天然耐药性(表1)17,18。此外,核苷酸和突变基序(定义为对不同类型抗逆转录病毒药物产生耐药性所需要的转换或颠换数量)的亚型差异 ,有可能影响耐药性的基因屏障19,20。例如,C亚型独特的标记密码子106多态性可促进V106M突变的发生。
核苷类逆转录酶抑制剂
在博茨瓦纳接受核苷类逆转录酶抑制剂(NRTIs)齐多夫定与去羟肌苷联合治疗的C亚型HIV感染病人,被发现有一个胸苷类似物突变 (TAM)途径(67N/70R/215Y)21,其在印度、南非或马拉维有C亚型(HIV感染)的病人中不常见到22-24。令人担心的是,在C亚型呈地方性流行地区的病人,在接受基于司他夫定或去羟肌苷的药物治疗方案后,K65R多核苷耐药突变和(或)K70E突变的发生率高(约为20%)24-26。在南非以司他夫定、去羟肌苷或齐多夫定作为核苷类骨干药物的一线或二线方案治疗后未产生疗效反应的病人中,7%~15%也被检出有K65R27,28。此外,来自以色列的多项研究报告,在来自埃塞俄比亚移民的C亚型病毒中,因治疗失败而出现高频K65R(突变) 29,而在印度10%~12%接受司他夫定、拉米夫定和奈韦拉平联合治疗(作为一线治疗)的病人携带K65R23。
由于治疗方案和疾病分期以及在许多发展中国家能够使用病毒负荷检测的情况不同,K65R 或TAMs的获取率存在某些差异是毋庸置疑的。这一点得到以下事实的强调:在一线治疗失败[通常与对M184V或NNRTI突变(K103 N/S、G190A、Y181V、K101E和V106A/M)的耐药性相关]后及时引入二线治疗,应防止TAMs或K65R的获取22,23。在埃塞俄比亚、巴西和撒哈拉以南非洲C亚型病毒的次级流行中的地区差异,也有可能影响耐药率,正如对NNRTIs耐药性所观察到的情况一样13,24,30。K65R突变谱的这些差异与亚型以及使用不恰当的药物治疗方案(而非地理因素)相关。
目前较新的(研究)工作表明,在C亚型中K65R获取率的增加有可能归因于C亚型RNA模板的性质而不是归因于例如病毒逆转录酶的亚型来源 31-33。尤其是,C亚型病毒有可能特别易于使密码子65上的事件暂停,从而促进逆转录期间的K65R获取32,33。相反,B亚型模板易于在密码子 67上频繁暂停,进而促进D67N和TAMs(而不是K65R)的产生32-34。
事实上,超敏焦磷酸测序法也已经显示,在某些尚未接受抗逆转录病毒治疗的人群中,K65R可作为少数物种被选择性传递35-37。新近获得C亚型病毒(感染)的病人比有B亚型感染而未曾接受治疗的病人有K65R的可能性显著更大(1.04%对0.25%,P<0.001)35,36。此外真实的情况是,K65R似乎更常出现在以下病人群中:有C亚型(病毒感染)并且含司他夫定、去羟肌苷或替诺福韦的治疗方案已经在他们中失败38。在某些情况下,C和CRF01_AE亚型中K65R的出现还与Y181C NNRTI突变相关27,39。相反,K65R有可能在A亚型中比在其他亚型中更少见 40。携带CRF-06_cpx重组病毒的布基纳法索病人获取TAMs的倾向比携带CRF02_AG重组病毒的病人高41。
非核苷类逆转录酶抑制剂
来自世界生组织(WHO)的最初指南建议使用单剂奈韦拉平来预防HIV母婴传播。在69%的C亚型妇女、36%的D亚型妇女、19%的A亚型妇女以及 21%的CRF02亚型妇女中观察到高频的耐药性,尽管在使用抗逆转录病毒治疗前没有耐药性 42-45。超敏检测法(可显示少数物种的耐药性)的使用已显示,有奈韦拉平—耐药突变(K103N和Y181C)病人的百分率甚至更高,达到有C亚型感染病人的70%~87%,相比之下达到有耐药突变的A亚型病人的42%46-48。这些结果强调了病毒亚型在促进耐药性出现中的作用,以下事实使耐药性加重:对NNRTIs的耐药性还可通过母乳喂养而得以传递 49。当前预防母亲传播的指南建议,采用三药联合方案来防止耐药性的出现50,51。
V106M突变常在C亚型病毒(在大约30%的病人中)暴露于奈韦拉平或依非韦仑后被选定,而V106A取代在其他亚型(暴露于)相同的NNRTIs 以后只有很少被选定(在大约5%的病人中)。这种情况归因于密码子106上逆转录酶的C亚型特异多态性52,53,并且在C亚型呈地方性流行的地区中已显示出有临床关联性(表1)21,23,54-58。尽管如此,在B亚型和C亚型中K103N和Y181C突变仍很重要,K103N(突变)发生于40%的 B亚型和29%的C亚型病毒中,以及Y181C(突变)发生于23%的B亚型和12%的C亚型病毒中59。在有C亚型病毒的病人中较常见的另一种取代是 G190A,后者还是自然发生G190A/S多态性的结果55。残基98上的逆转录酶多态性(常见于G亚型)还与B亚型中的NNRTI耐药性相关60。已有研究观察到,用依曲韦林(一种第二代NNRTI)时,在A、B和C亚型中的耐药途径仅有轻微差异54。
蛋白酶抑制剂
在奈非那韦(一种耐药性基因障碍低的药物)治疗失败的病人中,在G、CRF02_AG和CRF02_AE亚型分离株中不常观察到D30N突变(与B亚型病毒中的治疗失败相关)。相反, L90M途径有利于后面的亚型61。虽然来自以色列的埃塞俄比亚移民的C亚型病毒株支持L90M途径,但在博茨瓦纳有 C亚型病毒的病人确实有D30N(突变),表明来自埃塞俄比亚和南非的C亚型病毒或许有所不同62,63。有关B亚型中的D30N优势高于其他亚型的基础,有可能与B亚型中蛋白酶瓣区的灵活性以及弹性蛋白酶抑制剂复合物的去稳定作用(destabilization)相关,而为了在C亚型中挽救适合度(rescue fitness)并赋与耐药性有可能需要一种附加的N83T突变64,65。
在C、F和G亚型中观察到的L89M多态性还可以导致M89I/V突变,而且G亚型中的V82I多态性在治疗失败后出现I82 M/T/S耐药性显然很重要66(表1)。L90M耐药突变在来自巴西的B亚型中常见,但在F亚型中罕见67。在不同亚型的病毒中,蛋白酶36位的多态性有可能在决定是否出现特定的耐药突变方面起辅助作用68。
已有研究报告了非B亚型中蛋白酶基因多态性的差异。这些差异包括A亚型的蛋白酶残基10、20和63,C亚型的(蛋白酶)残基20、53、63、74 和82,D亚型的(蛋白酶)残基13和20,F亚型的(蛋白酶)残基10、14、20和77,G亚型的(蛋白酶)残基20、67、73、82和 88,CRF01_AE亚型的(蛋白酶)残基20、63、82和89,以及CRF02_AG亚型的(蛋白酶)残基2069,70。另外已有研究报告,与C 亚型相比,B亚型中NRTI和蛋白酶抑制剂耐药性突变出现率增高以及NNRTI突变的出现率相等71。在巴西南部,科学家报告,在C亚型中对蛋白酶抑制剂原发耐药性的相对发生频率低于B亚型72。然而,亚型的多样性不一定减少抗逆转录病毒疗法的最初益处,尽管有明确证据表明某些突变的优先出现,例如在某些非B亚型蛋白酶中的V82M,G亚型中的V82M(原文如此——编者注)对其他亚型中的V82A/F/S,或者B亚型中的N88D对C亚型和 CRF02_AG亚型中的N88S73。
蛋白酶抑制剂
重要突变还可损害NRTIs、NNRTIs和蛋白酶抑制剂在有关HIV-2病毒中的有效性,后者对若干种NNRTIs具有固有的耐药性(表 1)74,75。B亚型中蛋白酶的某些次要突变有可能显现为在数种非B亚型中频发的自然多态性(例如M36I和L89M)67,68,并且L89M多态性可以导致M89I对蛋白酶抑制剂的重要耐药性突变(表1)。有关奈非那韦和阿扎那韦的3项不同研究已发现,对于CRF02_AG重组病毒,野生型分离株的敏感性下降60,70,76。一项研究表明,A/G蛋白酶K26口袋的变形有可能是奈非那韦结合能较低以及A/G病毒敏感性较低的原因76。虽然已有研究识别出对某些蛋白酶抑制剂 (奈非那韦和阿扎那韦)敏感性较低的CRF02_AG分离株,但仅一项研究检出了野生型分离株中下降的阿扎那韦敏感性77。就奈非那韦的耐药性而言,竞争性检测支持较低的携带D30N的C亚型病毒的适合度,这能够解释某些C亚型分离株缺乏这种突变的原因65。
28 分钟前 上传
下载附件 (279.88 KB)
当HIV易受来自蛋白酶抑制剂的药物压力时,蛋白酶和gag基因可共同进化为一个功能单位。Gag中的突变可起代偿性取代作用,这种取代可增加对蛋白酶抑制剂的耐药率和耐药水平以及病毒的复制能力78。对于确定蛋白酶抑制剂的耐药性而言,目前尚无基因型系统可监测gag(的状态),尽管事实是,在 gag中的相关突变可使耐药性增高1~1.5倍,这取决于亚型。有可能的是,不同的亚型可能以不同的发生率发生代偿性gag突变。这或许最终构成在耐药性检测中进行gag基因分型的理由。
整合酶抑制剂
在以拉替拉韦(raltegravir)和以elvitegravir为主方案治疗失败的病人中,对整合酶抑制剂的耐药性与包括整合酶基因内 N155H、Q148K/R/H和Y143R/C部位上关键突变的3种主要途径相关,以及与有可能影响耐药性和病毒复制能力的亚型中的多态性相关 20,79-84。鉴于对这些化合物的耐药性有一种适度的基因屏障,临床治疗失败有可能由以下原因引起:使用了次最适治疗方案的骨干成分,或逆转录酶和蛋白酶耐药性的交互效应85,86。
HIV亚型中密码子140、148、151、157和160整合酶中的标记亚型差异,有可能影响耐药性的基因屏障20。这些变异可预示在C、 CRF02_AG和A/CRF01_AE亚型中发生G140S和G140C突变的基因屏障较高,以及在CRF02_AG和CRF01_AE亚型中发生 V151I突变的基因屏障也较高20,87。在35%的C亚型分离株中观察到E157Q和E160Q的突变基序,表明有亚型内的变异87。在各亚型中,密码子155和143 上的核苷酸基序得以高度保留20。这些观察结果提示,某些序列变异或许并不通过A、CRF02_AG和C亚型中的Q148R/H/K 和G140S 途径来提升耐药性20,87。尽管在HIV-2和HIV-1之间的整合酶序列中有40%的差异,但对拉替拉韦的耐药途径相似88。如果有人证实对整合酶抑制剂耐药的基因屏障在非B亚型中比在B亚型中高,则该结果在发展中国家可能有临床关联性20,87。
进入抑制剂
虽然将病毒(的细胞)进入作为靶点的药物仍处于开发的不同阶段,但env区的高水平多样性(20%~40%)预示,这类药物发生天然和突然出现耐药性的可能性将很可能较高。临床数据已显示,融合抑制剂恩夫韦肽由于高度保留了结合域而对非B亚型有活性,尽管HIV-2和HIV-1类O病毒对这种药物有天然的耐药性89,90。CCR5抑制剂马拉韦罗也对多种亚型有活性。
生物学和临床关联性
引人注目的生化数据和病毒学数据说明了遗传背景对HIV-1对抗逆转录病毒药物耐药的类型和程度具有差别效应,正如已得到证实的对NRTIs、 NNRTIs和蛋白酶抑制剂的耐药情况一样。对于蛋白酶抑制剂,遗传背景(包括每种亚型的多态性)可以影响原发性突变改变蛋白结合或蛋白酶功能的程度。因此,某些多态性可以起到与继发性耐药突变等效的作用。
重要的是,继续进行有关多态性在药物耐药性发生中的作用的研究。在一些病例中,药物暴露有可能导致这类多态性(例如逆转录酶中的A98G/S以及蛋白酶中的M36I、K20I和L89M)的扩增,从而导致了耐药的可能性91。在非洲的部分地区,已有研究报告,2年后在多达40%的病人中出现治疗失败 92。在印度已有研究报告,联合使用NRTIs和NNRTIs的一线治疗方案失败后,对两类药物的耐药率>80%93。人们还需要在多态性与药物耐药性之间可能存在相关性的背景下评估治疗前和治疗后的基因型的研究。该研究领域可能包括在不同的地理区域中,相同亚型变异体内多态性的变异性。在二线或三线治疗策略的背景下,这一信息也许提高了某些药物组合的有效性而超过其他的药物组合。
虽然在资源贫乏的国家抗逆转录病毒疗法的获得增加,但为了减少药物耐药性出现的长期临床益处,仍必须建立恰当的治疗策略。无论何种病毒亚型,使用无毒性的有效抗逆转录病毒药物都应产生优异的临床疗效反应。亚型差异、次最适疗法以及卫生保健实施系统的缺乏均可以创造耐药性加速发生的条件。另外仍有对低成本病毒载量监测的迫切需要,以便防止并检出药物的耐药性,并避免不必要的治疗转换94-96。
遗憾的是,有关耐药性的混合数据经常掩盖病毒亚型和抗逆转录病毒治疗的地区性差异在药物耐药性发生中的作用13。在资源贫乏的环境下,这类研究已使用了不同的NRTI骨干药物(例如齐多夫定和去羟肌苷、齐多夫定和拉米夫定或司他夫定与拉米夫定的组合)。还需要较大型的纵向研究以确定对一线抗逆转录病毒药物组合的疗效反应。研究者需要扩大治疗前和治疗后基因型耐药性检测的可获得性,以便包括所有使用抗逆转录病毒药物的国家。
表型分析尚未检出B亚型和非B亚型之间抗逆转录病毒药物敏感性的显著差异,该结果与用重组逆转录酶和蛋白酶获得的生化数据一致。这是确定无疑的理由,即所有的HIV亚型都应以或多或少等效的方式对好的药物治疗方案产生疗效反应。然而,某些非B(亚型)病毒的多态性有可能以其在暴露于抗逆转录病毒药物后在B亚型病毒中出现为基础,而起继发性耐药突变的作用,并且有可能经常难以推测这类多态性在非B亚型中的效应。例如,I93L取代可在C亚型中引起对某些蛋白酶抑制剂的高度敏感性,但在B亚型中可引起继发性耐药突变65。
虽然人们禁不住推测,耐药性的获取率可能对治疗有效性的耐久性有重要意义,但这种情况有可能仅适用于标准以下治疗方案的使用。例如,K65R突变的出现在C亚型比在B亚型中快19,27,并且生化机制可说明这种差异与HIV-1逆转录酶处理C亚型模板的方式有关31-33,97。在大约70%于博茨瓦纳(用)含去羟肌苷治疗方案失败的病人中25,以及在高比例(大约20%)于马拉维、印度和南非对司他夫定、拉米夫定和奈韦拉平未产生疗效反应的患者中也已经观察到有K65R38,98,99。
相反,在已接受替诺福韦或替诺福韦与恩曲他滨联用作为部分三重抗逆转录病毒药物疗法的B亚型和C亚型病人中,K65R并不常见27。虽然这种情况可反映出耐受性良好的有效药物的使用,这些药物细胞内半衰期长并且可以联合作用来抑制病毒复制和防止耐药突变的出现,但需要较大数量的病人和随访,以确定在C 亚型中K65R出现的任何一致效应是否有临床关联。K65R选择与奈韦拉平之间的强烈相关性,在针对K65R、Y181C和G190A/S突变所观察到的协同适合度(fitness)相互作用方面,也是令人担心的问题100-102。使用基于替诺福韦或齐多夫定的治疗方案,可以消除C亚型HIV感染中 K65R的出现103,104。
在药物中的交叉耐药性很重要,尤其是在治疗选择有可能受限的环境下。有关可获得的非B亚型中蛋白酶抑制剂的体外比较数据相对很少,然而这类数据有可能对了解蛋白酶抑制剂的交叉耐药性至关重要67,68。这类数据很重要,因为在资源有限的环境中,在一线或二线治疗失败后,蛋白酶抑制剂对药物测序而言经常是唯一可获得的选择。蛋白酶抑制剂耐药性(的发生)通常需要存在大量的耐药突变的事实,有可能意味着任何单一的突变对药物耐药性的作用都是微弱的,这是使用对耐药性发生有高基因屏障药物的一个优势。因此,有关药物耐药性的亚型间差异,有可能对NRTIs、NNRTIs和整合酶抑制剂比对蛋白酶抑制剂更重要。
总结
无论地理区域,一个需迫切优先考虑的全球性问题是优化HIV感染的治疗策略。令人欣慰的是,当前的抗逆转录病毒治疗策略似乎对广谱HIV亚型均有效。包括诸如司他夫定和去羟肌苷这类药物在内的次最适疗法可有助于K65R突变的选择,随后这可能限制许多二级治疗的选择。此外,次最适治疗方案使病人处于发生NNRTI耐药突变的危险中。了解非B亚型感染中的耐药模式可能有助于优化一线治疗方案的选择,并限制耐药性的获取。
6.合.彩!足球.篮球...各类投注开户下注
第一投注!现金网:招代理年薪10万以上:diyitouzhu.com |
|